HLAノックアウトiPS細胞
– ユニバーサルドナーセル –
B2M/CIITAダブルノックアウトHLA欠損iPS細胞のご紹介
製品名: StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO)
HLAノックアウトiPS細胞の背景
1.移植医療における免疫拒絶とHLA(ヒト白血球抗原)の役割
同種移植において、移植片(組織・細胞)に対するレシピエント(移植を受ける患者)の免疫系による拒絶反応は、依然として大きな課題です。この免疫拒絶の主たる原因は、細胞表面に発現するHLA(Human Leukocyte Antigen:ヒト白血球抗原)の型がドナーとレシピエント間で不一致であることです。HLAは、自己と非自己を識別する免疫システムにおいて中心的な役割を担っており、主に以下のクラスに分類されます。
- HLAクラス1 (Class I) : ほぼ全ての細胞表面に発現し、細胞傷害性Tリンパ球(CTL)が抗原提示を介して標的細胞を認識・攻撃する際の主要な分子です。
- HLAクラス2 (Class II) : 主に抗原提示細胞(マクロファージ、樹状細胞、B細胞など)に発現し、ヘルパーTリンパ球を介した免疫応答の調節に関与します。
2. iPS細胞を用いた細胞治療とゲノム編集技術の応用
iPS細胞(人工多能性幹細胞)は、再生医療や疾患モデル作製、創薬スクリーニングなど、多岐にわたる応用が期待されています。しかし、iPS細胞由来の細胞を移植する際にも、HLA型の不一致による免疫拒絶が問題となります。従来、HLAホモ接合体ドナー由来のiPS細胞バンクを構築することで、適合率を高め、免疫拒絶リスクを低減する試みがなされてきました。しかし、日本人で適合率の高いHLA型を持つドナーは限られており、多くの患者をカバーするには膨大な種類のiPS細胞株が必要となります。 近年、CRISPR/Cas9などのゲノム編集技術の発展により、iPS細胞のHLA遺伝子を改変し、免疫原性を低下させるアプローチが注目されています。HLAの発現を抑制または完全に欠損させることで、より多くの患者に適用可能な「ユニバーサルドナーセル」の作製を目指す研究が世界中で進められています。
3.HLA発現抑制のための標的遺伝子:B2MとCIITA
HLAの発現を効果的に抑制するために、以下の2つの遺伝子が主要なターゲットとして研究されています。
- β2ミクログロブリン(B2M)遺伝子: HLAクラス1分子の構成要素
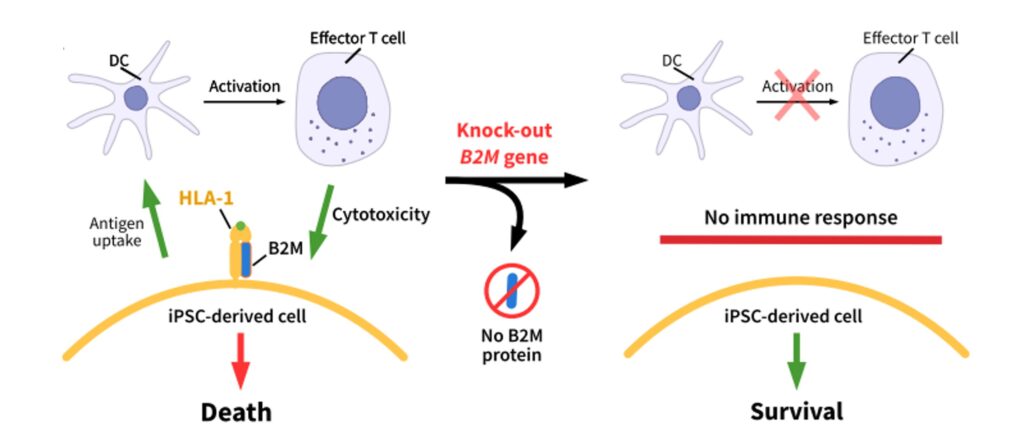
B2Mタンパク質は、HLAクラスI重鎖と結合し、その構造安定化と細胞表面への輸送に必須です。したがって、B2M遺伝子をノックアウト(KO)すると、HLAクラスI分子は細胞表面に正常に発現できなくなります(図1参照)。
- クラスII トランスアクチベーター(CIITA)遺伝子: HLAクラス2遺伝子のマスター制御因子
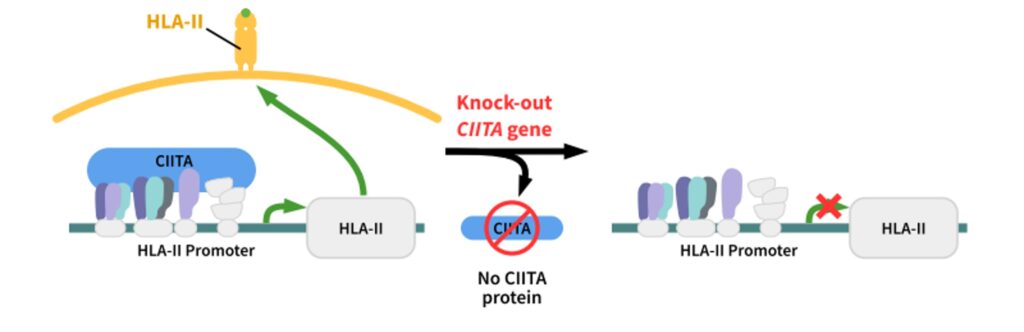
CIITAタンパク質は、HLAクラスII遺伝子群の転写を制御するマスターレギュレーターです。CIITA遺伝子をノックアウトすると、HLAクラスII分子の発現が誘導されなくなります(図2参照)。
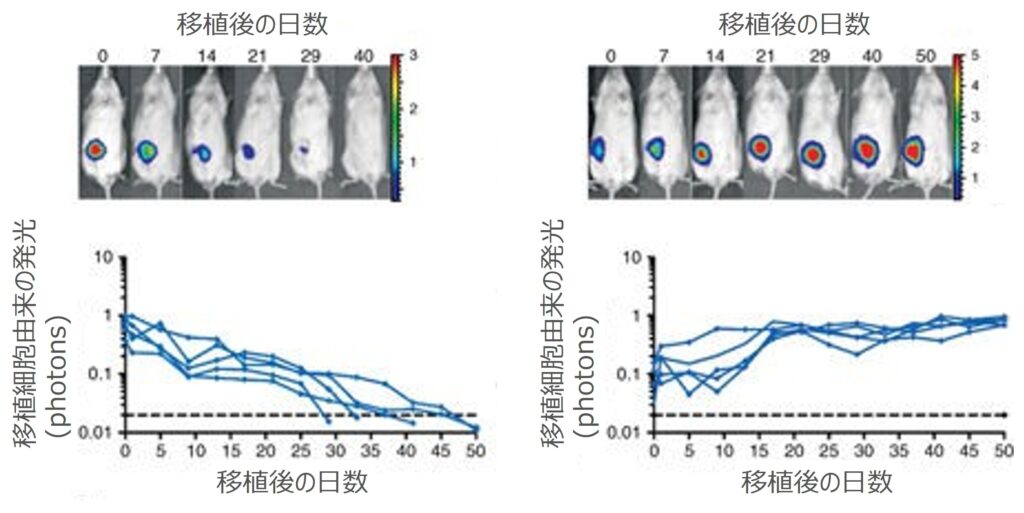
これらの遺伝子を標的とした研究は、HLAノックアウトiPS細胞の有用性を裏付けています。例えば、Deuseらの研究では、B2MおよびCIITA遺伝子をダブルノックアウトし、さらに免疫チェックポイント分子CD47を過剰発現させたマウスおよびヒトiPS細胞由来細胞が、免疫担当マウスへの同種移植において拒絶を回避し、長期的に生着することが示されました(参考文献2)。また、Wangらは、B2M/CIITAダブルノックアウトヒトiPS細胞由来細胞をサルに移植し、免疫応答の抑制と治療効果の促進を確認しています(参考文献3)。これらの研究成果は、B2M/CIITAダブルノックアウトによるHLAクラス1/2同時欠損が、iPS細胞由来細胞の免疫原性を効果的に低減させる戦略であることを強く示唆しています。
リプロセルのHLAノックアウトiPS細胞株
StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO)
リプロセルは、最先端のゲノム編集技術を駆使し、高品質なHLAノックアウトiPS細胞株を開発しました。お客様の研究ニーズに合わせ、以下の2製品を提供しております。
- B2M/CIITA ダブルノックアウト iPS細胞株
StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO)
HLAクラス1およびクラス2の両方の発現を抑制。
- B2M ノックアウト iPS細胞株
StemEdit™ Human iPSC non-HLA class 1 (B2M Homo KO)
HLAクラス1の発現を抑制。
これらの細胞株をご利用いただくことで、お客様自身でゲノム編集を行う手間なく、直ちにHLAノックアウトiPS細胞を用いた研究を開始できます。両株ともに、標的遺伝子(B2M、CIITA)の両アレル(ホモ接合型)でノックアウトされており、HLAの発現を確実に抑制します。
【本製品の特長】
- 高品質なゲノム編集: 独自の高効率ゲノム編集技術(CRISPR/Cas9とは異なる手法)を採用。
- ホモ接合型ノックアウト: 標的遺伝子の両アレルに変異を導入し、確実な発現抑制を実現。
- ライセンス: 動物実験を含む基礎研究目的での使用には、追加のライセンスは原則不要です。(商用利用・臨床応用をご検討の場合は、別途ご相談ください。)
- 臨床グレード由来: 高品質な臨床グレードiPS細胞株を親株として使用。
参考文献
- Zhang Q, et al. Concise Review: One Stone for Multiple Birds: Generating Universally Compatible Human Embryonic Stem Cells. Stem Cells. 2016;34(9):2269-2275. doi:10.1002/stem.2423
- Deuse T, et al. Hypoimmunogenic derivatives of induced pluripotent stem cells evade immune rejection in fully immunocompetent allogeneic recipients. Nat Biotechnol. 2019;37(3):252-258. Correction published Nat Biotechnol. 2022 Nov;40(11):1690. doi:10.1038/s41587-019-0016-3
- Wang B, et al. Diminished expression of major histocompatibility complex facilitates the use of human induced pluripotent stem cells in monkey. Stem Cell Res Ther. 2020;11(1):334. doi:10.1186/s13287-020-01847-1
製品情報
製品リスト
| 品番 | 製品名 | 株名 | ノックアウト 遺伝子(部位) |
|---|---|---|---|
| RCRP043E | StemEdit Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO) | VCT-37-F35-E1 | B2M (NM_004048.4: c.106_107del) CIITA (NM_000246.4: c.587_594del) |
| RCRP044E | StemEdit Human iPSC non-HLA class 1 (B2M Homo KO) | VCT-37-F35-C5 | B2M (NM_004048.4: c.106_107del) |
用途:本製品は研究用です。診断・治療目的での使用はできません。臨床応用をご検討の場合は、別途ご相談ください。
品質データ
1.核型解析
「StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO)」(RCRP043E) および「StemEdit™ Human iPSC non-HLA class 1 (B2M Homo KO)」(RCRP044E) の核型解析を実施し、両株ともに正常な核型 (46, XX ) を維持していることを確認しました。(図4にRCRP043Eの結果を示す)
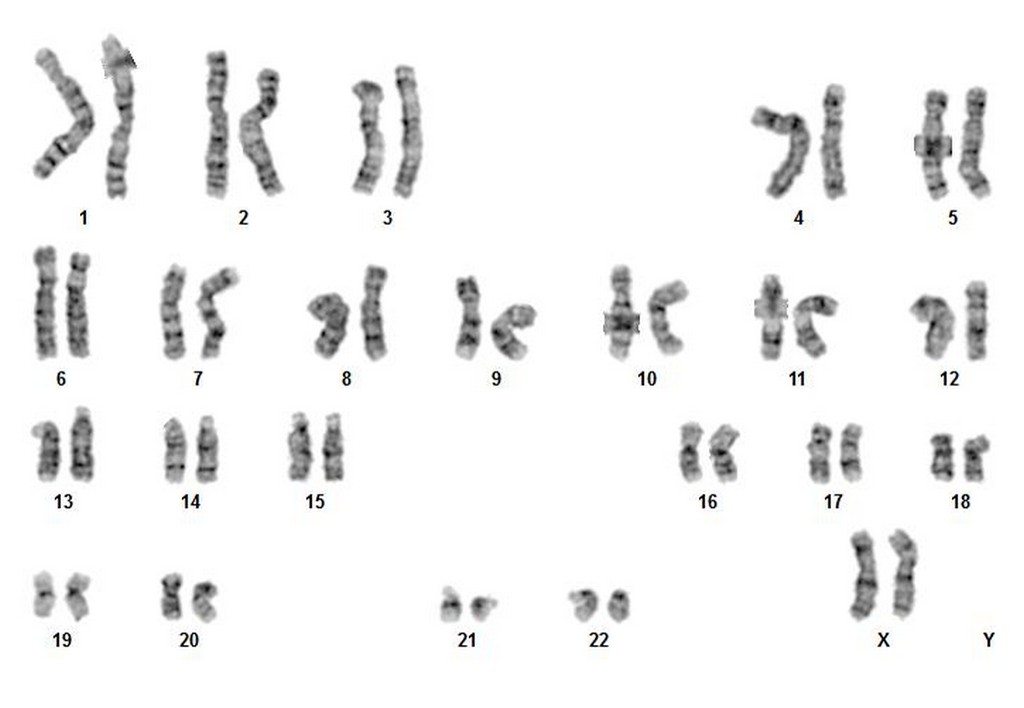
StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO) (RCRP043E) の核型解析 (G-banding)の結果、正常核型を確認した。
2.未分化マーカーの発現
両株について、未分化マーカーであるSSEA-4およびNanogの発現を免疫蛍光染色法にて確認しました。いずれの株においても、これらの未分化マーカーが陽性であることを確認しています。(図5にRCRP043Eの結果を示す)
B2M/CIITAダブルノックアウト株
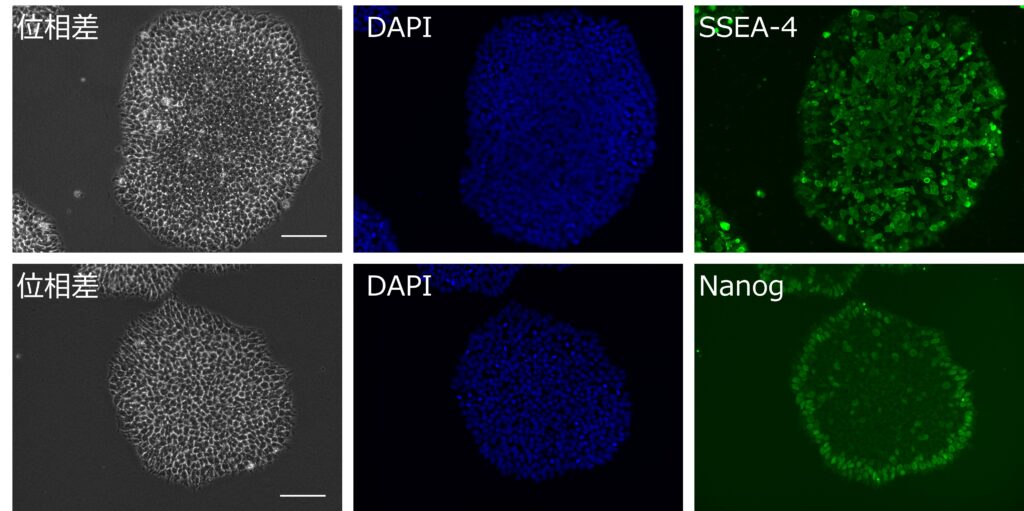
左:位相差像、中:DAPI(核)、右上:SSEA-4、右下:Nanog。スケールバー=100 µm。
3.HLA クラス1の発現抑制確認
両株および親株(VCT-37-F35)におけるHLAクラス1の発現レベルを、抗HLA-ABC抗体を用いたフローサイトメトリー解析により評価しました。親株ではHLAクラスIの発現が確認されましたが、B2M遺伝子がノックアウトされているRCRP043EおよびRCRP044Eでは、HLAクラスIの発現が顕著に抑制されていることを確認しました。(図6に親株とRCRP043Eの比較結果を示す)
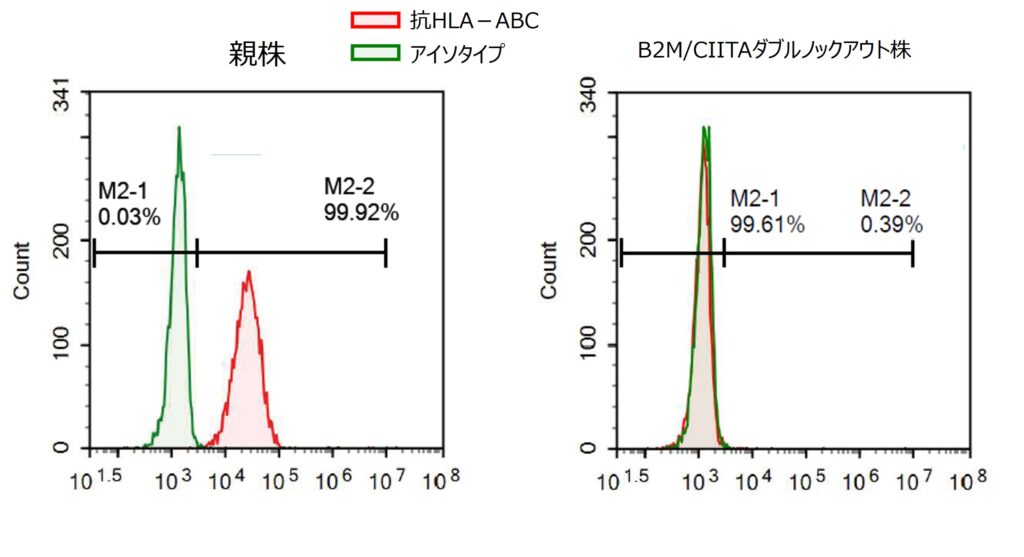
左:親株 (VCT-37-F35)、右:StemEdit™ Human iPSC non-HLA class 1/2 (B2M/CIITA Homo double KO) (RCRP043E)。ダブルノックアウト株においてHLAクラス1の発現抑制が確認された。
高品質な親株:臨床グレードiPS細胞株 VCT-37-F35
本HLAノックアウトiPS細胞株の作製には、リプロセルが樹立した臨床グレードiPS細胞株「VCT-37-F35」を親株として使用しています。当社の臨床グレードiPS細胞は、以下の特長を有しています(参考サイト)。
- 規制準拠: 日本、米国、欧州の規制要件を考慮したプロセスで開発・製造されています。
- 厳格なドナースクリーニング: 倫理的配慮のもと、適切なスクリーニングを経た健常人ドナー由来の体細胞を使用しています。
- GMP準拠施設での製造: 特定細胞加工物製造許可を取得した施設(神奈川県川崎市 ライフイノベーションセンター内、施設番号:FA3200006)にて、SOP(標準作業手順書)に基づき、厳格な品質管理下で製造・凍結保存されています(図7、8)。
- 高い安全性: iPS細胞樹立には、ゲノムへの挿入リスクがないmRNAを用いた「RNAリプログラミング法」を採用。導入遺伝子の残存リスクを最小限に抑え、高い安全性を確保しています。
当社の臨床グレードiPS細胞は、国内外の企業や研究機関における再生医療等製品開発に広く利用されています。例えば、提供先のGameto社(米国)では、当社のiPS細胞を用いた不妊治療技術「Fertilo」の開発を進めており、米国FDAより第3相臨床試験のIND(新薬臨床試験開始届)承認を取得するなど、実用化に向けた動きが加速しています(参考サイト)。

1階に特定細胞加工物製造施設を設置。

トレーニングを受けた専任の作業員がSOPに基づき、厳格な管理下で作業を実施。
 Global
Global
